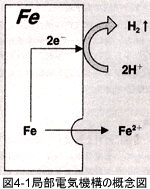
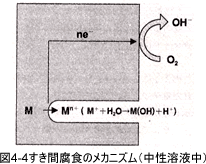
�ȏ�q�ׂĂ��܂����悤�ɕ��H�����͓d�C���w�����ł���A�J�\�[�h�����ƃA�m�[�h�����Ƃł̓d�q�̂����ɂ�蕅�H���i�ނ��ƂɂȂ�܂��B���H��}����i�h�H�j���߂ɂ͂܂����̕��H�̃��J�j�Y����������m�邱�ƁA�܂�Z�Ў����ł͂ǂ̌��f���n�����Ă��邩�A���Ɏ����ł͂ǂ̂悤�Ȕ������N�����Ă��邩�����邱�Ƃ���n�܂�܂��B���ɂ��̔������x�z���Ă�����̂𐧌䂵�Ă������Ƃɂ�蕅�H��h�~���܂��B�]���܂��Ėh�H���@�͌����I�ɂ́A�J�\�[�h�A�A�m�[�h�����̈���܂��͗����𐧌䂷����@�Ƃ����܂��B
1.�J�\�[�h�h�H�@
��ʂɗn�t���ł̃J�\�[�h�����́A���f�����^�i4.2���j�Ǝ_�f����^�i4.6���j�ɕ������܂��B
�ipH�ɂ��h�H�j
pH�̒ቺ�ƂƂ��ɐ��f�C�I���Z�x�͑�������̂ŁA���f�����^�̃J�\�[�h�������x���傫���Ȃ�܂��B�]���܂��Ď_�����͋C�ł̎g�p�͍D�܂�������܂���B�����n�t�ł��\����Ǐ��I��pH��������Ǖ����H���邱�Ƃ�����A���A�\���ɑ��钍�ӂ��K�v�ƂȂ�܂��B
�i�n���_�f�ʂɂ��h�H�j
�_�f����^�̃J�\�[�h�����ł́A�n�t���̗n���_�f�̊Ҍ���������Ȕ����ƂȂ�܂��B���̔�����}������ɂ́A�_�f�Z�x��������A�_�f�g�U��}��������@���l�����܂��B�O�҂͉Ȋw�I��i�ɂ��n���_�f������������@��A�ϕ�����i���x���オ��Ǝ_�f�n��ʂ���������j���@�A��҂ł͗n�t�̗�����}���_�f�̊g�U��h�~���铙������܂��B
2.�A�m�[�h�h�H�@
�i�d�ʂɂ��h�H�j
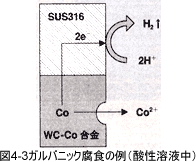
�K���o�j�b�N���H�i4.2-2�j����悤�ȏꍇ�ł́A���H��h�~�������ޗ��̓d�ʂ��M�ɐݒ肷��K�v������܂��A���̓d�ʂ͕��ɋȐ��i3.2�j�ɂ�苁�߂邱�Ƃ��ł��܂��B�����ȓd�ʂ̍��ł�����ނƂ̖ʐϔ�ɂ���Ă͑傫�ȕ��H�d��������邱�Ƃ����蒍�ӂ��K�v�ƂȂ�܂��B
�d�ʂ��M�ȕ��փV�t�g������@�Ƃ��Ă͍������ɂ����@������A���d�����ł�������������������������@�Ȃǂ��Ƃ��Ă��܂��B
�i�s���Ԕ햌�`���ɂ��h�H�j
�����̗n���ł͖{���̊����������ċM�����̂悤�ȓ����������悤�Ȍ��ۂ�����܂��B����͋������\�ʂɎ_�����A���_�������̔햌���`�����A�\�ʂ���̊����n����j�~����悤�Ȍ��ۂł���s���ԂƌĂ�A���̔햌�͕s���Ԕ햌�ƌĂ�Ă��܂��B���̌��ۂ����ɋȐ��i3.2�j�ɂ��m�邱�Ƃ��ł��A�����v��d�v�ƂȂ�܂��B���̋Z�p�͓S�|�ނł͍|��Ni,Cr����Y�����X�e�����X�|�Ƃ��邱�Ƃł悭�m���Ă��܂����A���d�����ł�������������Co����Ni�ɂ�����A����Ɏ_���������₷��Cr�AMo��Y��������@��A����ɂ͌�������Ti�Ƃ�����@���Ƃ��Ă��܂��B
�i���̑��̖h�H�@�j
�Č��d���ނł͕\�ʂɃ|�A�⌇�ׂ�����ƁA�����Ō��ԕ��H����������A�\�ʃG�l���M�[�̍��ɂ�芈�������ėn�������肵�܂��B�[�����k���������邽�߂ɏČ������̌�����HIP�����ɂ���k�������d�v�ƂȂ�܂��B�܂��J�\�[�h�A�A�m�[�h��������h�~���邽�߂ɕ\�ʂ����S�ɔ핢���Ă��܂��R�[�e�B���O����������܂��B
�܂��d���ނ��g�p���鑤�ɂ����܂��Ă��A�Ⴆ�Ό����͌���t��@�����A�ۊǂɂ������Ă͎��x�̒Ⴂ�ꏊ�ɕۊǂ���A�h�K������h�z���铙���ɑ������K�v�ɂȂ�܂��B